4.3. Karta BLOZ
Aby wyświetlić kartę wybranego towaru, należy podświetlić wybraną pozycję i kliknąć Podgląd (karty BLOZ nie można edytować, co ma na celu zachowanie spójności przechowywanych danych).
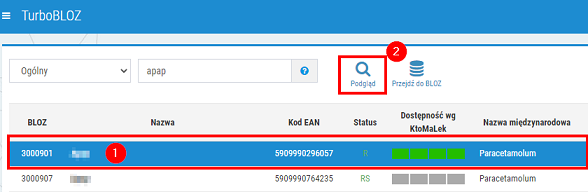
Rys. 1. Podgląd karty BLOZ
Kartę BLOZ można wyświetlić w dwóch wariantach (użytkownik decyduje, którą wersję chce wyświetlić za pomocą pola Klasyczna karta BLOZ – gdy pole jest zaznaczone, to widoczna jest karta klasyczna, gdy pole jest odznaczone, to wyświetlana jest nowa karta):
- klasyczna karta BLOZ – karta prezentuje podstawowe informacje o produkcie oraz o jego odpłatnościach:
Klasyczna karta BLOZ:
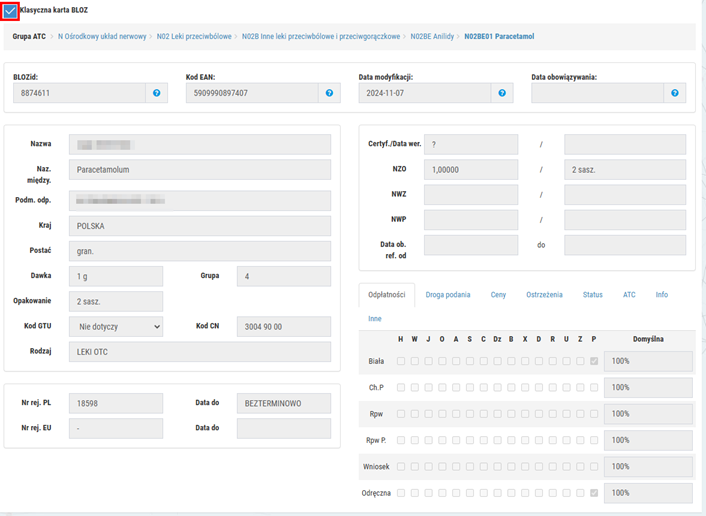
Rys. 2. Klasyczna karta BLOZ, przykład
- nowa karta BLOZ – uproszczony widok najważniejszych informacji dotyczących danego towaru w jednym miejscu:

Rys. 3. Przykładowa karta BLOZ
Po prawej stronie okna użytkownik ma dostęp do historii zmian na danej karcie, dzięki czemu można sprawdzić jak karta wyglądała w dowolnym momencie w przeszłości. Podczas przeglądania zmian historycznych na danej karcie, pola, które uległy zmianie zostaną wyróżnione kolorem, np.:
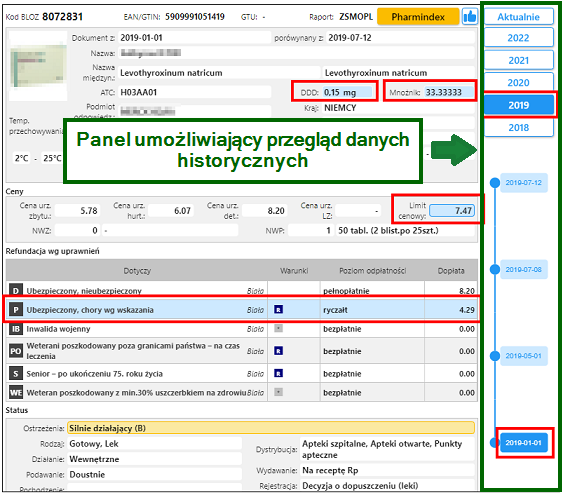
Rys. 4. Historia zmian na danej karcie
Pola na karcie BLOZ
- BLOZid - unikalny identyfikator produktu nadawany w ramach BLOZ,
- kod EAN - kod kreskowy identyfikujący lek,
- data modyfikacji - data ostatniej modyfikacji danych opisujących daną pozycję w bazie BLOZ,
- data obowiązywania - data wejścia w życie zmian urzędowych,
- nazwa,
- nazwa miedz. - nazwa międzynarodowa leku,
- podmiot odp. - podmiot gospodarczy odpowiedzialny prawnie za wprowadzenie produktu leczniczego do obrotu,
- kraj - kraj, w którym został wyprodukowany lek,
- postać - postać, pod jaką występuje dany lek. Ten sam lek występujący także pod inną postacią posiada w bazie BLOZ inny numer,
- dawka - określa dawkę leku,
- opakowanie - opakowanie, w jakim sprzedawany jest dany lek. Ten sam lek występujący w opakowaniu zawierającym inną ilość tego leku posiada inny numer BLOZ,
- grupa - grupa leku (Grupy leku),
- kod GTU – symbol grupy towarowo-usługowej,
- kod CN (Nomenklatura Scalona) – symbol klasyfikacji towaru na potrzeby VAT,
- numer rejestru PL, data do - numer rejestru wg Urzędowego Wykazu Środków Farmaceutycznych i Materiałów Medycznych dopuszczonych do obrotu w Polsce lub numer świadectwa dopuszczenia do obrotu i data wycofania leku z obrotu (możliwa opcja bezterminowo),
- numer rejestru UE, data do - numer rejestru dla produktu w Unii Europejskiej i data wycofania leku z obrotu w UE (możliwa opcja bezterminowo),
- droga podania - informacje o sposobie podawania leku,
- certyfikat - certyfikat, jeżeli T - tak, jeżeli N - nie,
- data weryfikacji - data weryfikacji posiadania certyfikatu,
- NZO - najmniejsze zarejestrowane opakowanie (mnożnik / opis),
- NWZ - najmniejsze zarejestrowane opakowanie w wykazach zwykłych (mnożnik / opis),
- NWP - najmniejsze zarejestrowane opakowanie w wykazach leków na choroby przewlekłe (mnożnik / opis),
- data ob. refundacji od, data ob.refundacji do - data obowiązywania refundacji na dany towar.
Pozostałe informacje dotyczące leku zostały rozdzielone pomiędzy zakładki:
- odpłatności (Odpłatności i rodzaje recept)- rodzaj odpłatności podczas sprzedaży na receptę danego koloru. Dany lek może być sprzedawany na receptę danego koloru za określoną odpłatność tylko wtedy, gdy znacznik -
 znajduje się na przecięciu wiersza odpowiadającego kolorowi recepty i kolumny odpowiadającej rodzajowi odpłatności;
znajduje się na przecięciu wiersza odpowiadającego kolorowi recepty i kolumny odpowiadającej rodzajowi odpłatności; - droga podania - informacje o sposobie podawania leku;
- ceny:
- cena urz. det. - cena urzędowa detaliczna, określana w stosownym obwieszczeniu ogłaszanym przez właściwego ministra do spraw zdrowia,
- cena urz. hurt. - cena urzędowa hurtowa,
- cena zbytu - cena urzędowa zbytu,
- limit cenowy - limit ceny określany w stosownym obwieszczeniu ogłaszanym przez właściwego ministra do spraw zdrowia,
- stawka VAT - podatek od towarów i usług,
Pola związane z kwotami zapłat pacjentów:
- zapłata BZ dla odpłatności BZ (bezpłatna),
- zapłata 30% - dla odpłatności 30%,
- zapłata Rycz. - dla odpłatności ryczałtowej,
- zapłata 50% - dla odpłatności 50%;
- Wysokość kaucji zwrotnej – wartość kaucji towaru uczestniczącego w systemie kaucyjnym (Dziennik Ustaw 2024 r. poz. 1911). Należy pamiętać, że w BLOZ znajdą się informacje wyłącznie o tych produktach kaucyjnych, które zostaną zarejestrowane w BLOZ przez producentów wprowadzających dane towary na rynek. Informacją, że dany produkt podlega kaucji, jest logo na opakowaniu
 lub
lub  . System kaucyjny zacznie obowiązywać w Polsce od 1 października 2025 r. Opakowania kaucyjne będą miały inny BLOZ i EAN niż te same produkty ze „starszych” dostaw.
. System kaucyjny zacznie obowiązywać w Polsce od 1 października 2025 r. Opakowania kaucyjne będą miały inny BLOZ i EAN niż te same produkty ze „starszych” dostaw.
- ostrzeżenia (Ostrzeżenia) - zakładka zawiera informacje na temat leku, które (w zależności od konfiguracji programu) mogą być wyświetlane podczas sprzedaży wybranego towaru, aby zwrócić uwagę sprzedawcy o specyficznych właściwościach danego preparatu;
- status - zakładka zawiera szczegółowe informacje o wybranym leku, np. o jego pochodzeniu, sposobach dystrybucji, sposobie działania itd. Widoczna jest lista kategorii, pomiędzy które podzielono informacje. Informacje wchodzące w skład wybranej kategorii stają się widoczne dopiero po rozwinięciu tej kategorii (Listy rozwijane) i jeżeli jakieś informacje dotyczą wybranego leku, oznaczone są znacznikiem -
 ;
; - ATC - kody ATC to system kodów (Anatomiczno Terapeutyczno Chemicznych), w którym leki są przyporządkowane do różnych grup w zależności od ich przeznaczenia oraz właściwości chemicznych, farmakologicznych i terapeutycznych. W celu leczenia głównego wskazania podawane są: mnożnik DDD oraz wartość DDD - przypuszczalna dawka dobowa leku;
- info - dodatkowe informacje o leku;
- inne - w zakładce znajdują się dodatkowe informacje np.:
- Ilość w opakowaniu – ilość leku w opakowaniu;
- Temperatura przechowywania,
- Czy raportować lek do ZSMOPL – znacznik raportowania do ZSMOPL;
- Wyłączony ze sprz. weter. – towar oznaczony jako wyłączony ze sprzedaży na receptę weterynaryjną (dot. środków przeciwdrobnoustrojowych i grup środków przeciwdrobnoustrojowych wymienionych w załączniku Rozporządzenia Wykonawczego Komisji (UE) 2022/1255 z dnia 19 lipca 2022);
- Lek lub subst. wytw. w RP – lek wytwarzany na terytorium Rzeczypospolitej Polskiej albo gdy do jego wytworzenia wykorzystano substancję czynną wytworzoną na terytorium Rzeczypospolitej Polskiej (lista tzw. „polskich leków” ze zniżką -10%, wykaz G1);
- Lek i subst. wywt. w RP – lek wytwarzany na terytorium Rzeczypospolitej Polskiej z wykorzystaniem substancji czynnej wytwarzanej na terytorium Rzeczypospolitej Polskiej (lista tzw. „polskich leków” ze zniżką -15%, wykaz G2).